إليك عزيزي الطالب طريقة حساب الرقم الهيدروجيني pH بمحاليل الأحماض و القواعد :
بماأن الأحماض القویة تتأین تأین تاما لذلك فأن هذه الأحماض في المحالیل المخففة(0.1M ≥) أ و(0.1N ≥) ، یمكن اعتبار تركیز ها تركیز أیون الهیدروجین H+ بذلك یمكن حساب قیمة(pH) لهذه الاحماض على النحو التالي:
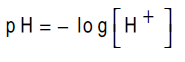
ثانيا القاعدة القویة:
ما ینطبق على الحمض القوى ینطبق على القاعدة القویة حیث یعبر عن تركیز القاعدة بتركیز أیون الهیدروكسید للقواعد التي تحتو ى على أیون OH- بذلك یمكن حساب قیمة (pOH) على النحو التالي:
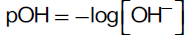
ومنها یمكن حساب قیمة (pH)كالآتي:
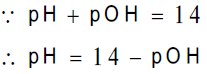
ثالثا الحمض الضعیف:
وهو حمض غیر تام التأین مثل معظم الأحماض العضویة فأن عیاریة الحمض تزید عن تركیز أیون الهیدروجین : ویتم حساب قیمة(pH) لهذه الأحماض كالآتي
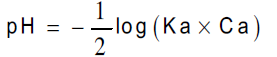

رابعا القاعدة الضعیفة:
هي قاعدة غیرتامة التأین وبذلك نجد أن تركیزها یزید كثیرا عن تركیز أیون الهیدروكسید ويتم حساب قيمة PH لهذه القواعد كالآتي

هل تعلم؟ نحن في منصة اسأل المنهاج نجيب على اسئلة الطلاب من جميع الدول العربية، كل ما عليك فعله هو طرح سؤالك من خلال الزر في الأعلى ويمكنك العودة الينا مرة اخرى من خلال البحث في جوجل عن "اسأل المنهاج"، لا تقم بنقل المحتوى دون ذكر المصدر جميع الحقوق محفوظة لمنصة اسال المنهاج
